חוקרים בפקולטה לביולוגיה בטכניון פענחו מבנה תלת מימדי, ברמה אטומית, של פפטיד אנטיבקטריאלי בשם יופרין 3.5, המופרש על גבי עורה של קרפדה אוסטרלית כחלק ממערכת החיסון שלה, וגילו שהוא יוצר, על ידי התארגנות עצמית, מבנה סיבי ייחודי. מעבר לכך, הם גילו שיש לסיב המיוחד מנגנון התאמה מבנית מתוחכם המספק לקרפדה הגנה אקטיבית בנוכחות החיידקים התוקפים אותה. הבנת המבנה של פפטיד זה ומנגנון פעילותו עשויים לסייע בפיתוח תרופות אנטיבקטריאליות יעילות, יציבות, ומופעלות רק במקרה של נוכחות חיידקים. את המחקר שהתפרסם בכתב העת PNAS הובילו פרופ' מיטל לנדאו, ד"ר ניר סלינס וד"ר עינב טייב-פליגלמן תוך שיתוף פעולה עם עמיתיהם בישראל ובספרד.
החוקרים בטכניון הסבירו כי המבנה של הסיב האנטיבקטריאלי מהקרפדה מזכיר סיבים עמילואידיים המוכרים לעולם הרפואה בהקשר של מחלות נוירו-דגנרטיביות כגון אלצהיימר ופרקינסון. במחלות אלה, הסיבים העמילואידיים מצטברים במוח וגורמים לפגיעה בתפקודי המוח באופן הדרגתי. עם זאת, בשנים האחרונות התברר שסיבים עמילואידיים מסויימים יכולים למלא תפקידים שונים לטובת האורגניזם המייצר אותם, החל באדם וכלה במיקרובים. לדוגמא, חיידקים מסוימים מייצרים סיבים כאלה כנשק המשמש אותם לפגיעה בתאי האורגניזם המארח.
קבוצת המחקר של פרופ' לנדאו אחראית לאחת מפריצות הדרך בהקשר זה – פענוח ראשון של המבנה התלת-ממדי של סיבי עמילואיד בחיידקיים. פרופ' לנדאו פרסמה את המבנה החדש, הנקרא cross-α, בכתב העת Science בשנת 2017. באותו מאמר הוצג הסיב העמילואידי בחיידק הסטפילוקוק הזהוב (Staphylococcus aureus) ותואר תפקודו ככלי נשק ("חץ רעיל") המגביר את אלימותו של החיידק כלפי מערכת החיסון.
5 צפייה בגלריה
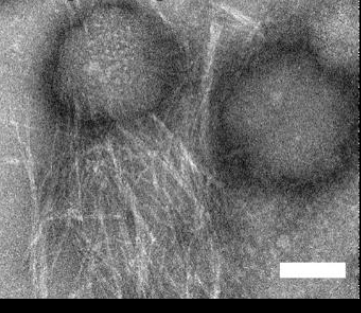

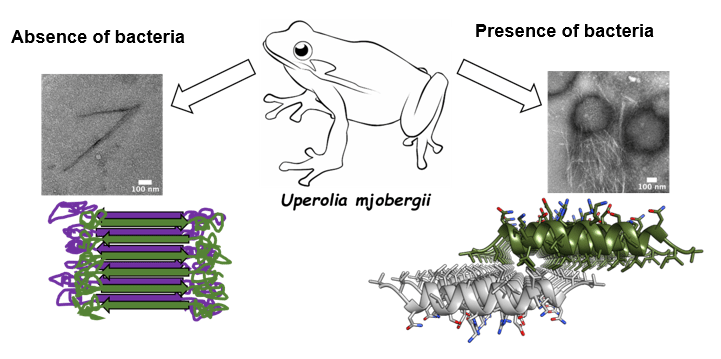
הפפטיד יופרין 3.5 מופרש על עור הקרפדה בתצורה "רדומה", בה מולקולות הפפטיד מתארגנות לכדי סיב עמילואידי מסוג cross-β. בעת חשיפה לחיידקים יש האצה של יצירת סיבים מסוג cross-α על גבי קרומי התא של אותם חיידקים שמובילים להרג. התמונות נלקחו באמצעות מיקרוסקופ אלקטרונים חודר (TEM) במרכז למיקרוסקופיית אלקטרונים בפקולטות להנדסת חומרים ולהנדסה כימית בטכניון. המבנה האטומי cross-α נקבע באמצעות מאיץ החלקיקים האירופי בצרפת (ESRF)
(צילום: ניר סלינס, טכניון)
המנגנון שהם מציעים כיום מתאר את הפפטיד האנטיבקטריאלי המופרש על גבי עור הקרפדה בתצורה "רדומה" שאינה פעילה כנגד חיידקים, בה מולקולות הפפטיד מתארגנות לכדי סיב עמילואידי מסוג cross-β, המאופיין ביציבות גבוהה ולכן נשמר היטב. סיבים אלה מהווים "מאגר" של מולקולות תקיפה פוטנציאליות המתעוררות בשעת הצורך. בעת חשיפה לחיידקים, אותם הפפטידים באים במגע עם מולקולות השומן של קרומי התא של החיידקים, כתוצאה מכך מתרחש שינוי מבני והסיב הופך לתצורת cross-α – אותה תצורה שקבוצת המחקר גילתה ב-2017. שינוי זה הופך את הסיב לכלי נשק קטלני המחסל את החיידקים התוקפים את עור הקרפדה. "זהו מנגנון הגנה מתוחכם של הקרפדה, שמופעל ע"י החיידקים עצמם שתוקפים אותה" – אומרת פרופ' לנדאו. "זוהי דוגמה ייחודית לתכנון אבולוציוני של שינוי במבנה סופרה מולקולרי כדי לבקר פעילות".
כיוון שפפטידים אנטימיקרוביאליים קיימים בכל הממלכות בעולם החי, יש בסיס להנחה שהם נוצרו בשלבים מוקדמים באבולוציה, ומהווים כלי נשק נפוץ בטבע. מחקר זה תורם רבות להבנת מנגנוני פעולה חדשניים של פפטידים אנטימיקרוביאליים, ששותפים לא רק בבלימת זיהומים חיידקיים אלא גם בהרג תאים סרטניים. יותר מכך, תגלית זו תורמת להבנה מעמיקה יותר של התפקיד הפזיולוגי והתכונות של סיבים העמילואידים הקשורים במחלות נוירו-דגנרטיביות.
החוקרים מקווים כי התגלית המדעית תוביל ליישומים רפואיים וטכנולוגיים, בין השאר בהקשר של המאבק המורכב בהתפתחות עמידות חיידקית לאנטיביוטיקה. להערכתם, יתכן שמנגנון ההשתנות המתוחכם של פפטיד הקרפדה יספק השראה לפיתוח פפטידיים מלאכותיים שיהיו יעילים יותר ויציבים יותר מטיפולים קיימים בחיסול זיהומים חיידקיים מזיקים ומסוכנים, ועבור ציפוי יציב של מכשור רפואי, שתלים, וציוד תעשייתי, שיופעל רק במקרה של נוכחות חיידקים. פרופ' לנדאו היא גם חברת סגל בפקולטה לביולוגיה ומזון וחברה ב- EMBL - המעבדה האירופית לביולוגיה מולקולרית בהמבורג.